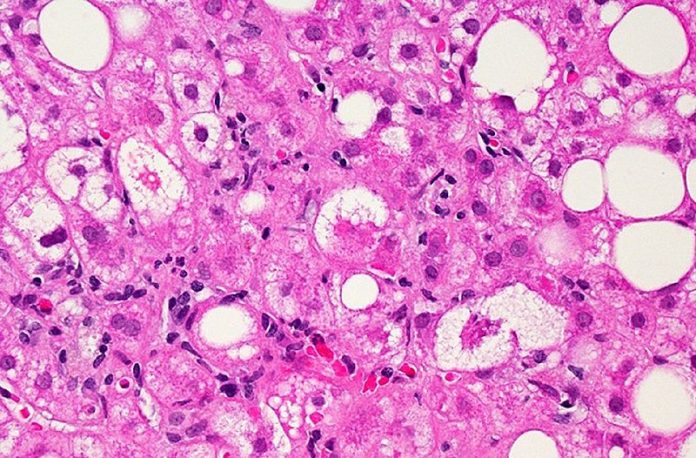
Rezdiffra (resmetirom) została zatwierdzona przez FDA w USA do leczenia osób dorosłych z niealkoholowym stłuszczeniowym zapaleniem wątroby (NASH) bez marskości wątroby i umiarkowanym do zaawansowanego bliznowacenia wątroby (zwłóknieniem), do stosowania wraz z dietą i ćwiczeniami fizycznymi.
Do tej pory pacjenci z niealkoholowym stłuszczeniowym zapaleniem wątroby (NASH), bez marskości wątroby, u których występowało również znaczne bliznowacenie wątroby, nie mieli leków, które mogłyby bezpośrednio pomóc w ich leczeniu. uszkodzenie wątroby. FDA zatwierdzenie przez firmę Rezdiffra po raz pierwszy umożliwi: leczenie opcją dla tych pacjentów, oprócz diety i ćwiczeń fizycznych.
NASH jest wynikiem progresji bezalkoholowej tkanki tłuszczowej wątroba choroba gdzie wątroba zapalenie z czasem może prowadzić do bliznowacenia wątroby i dysfunkcji wątroby. NASH często wiąże się z innymi problemami zdrowotnymi, takimi jak wysokie ciśnienie krwi i cukrzyca typu 2. Według co najmniej jednego szacunku około 6–8 milionów ludzi w USA ma NASH z umiarkowanym lub zaawansowanym bliznowaceniem wątroby i oczekuje się, że liczba ta będzie rosnąć.
Rezdiffra jest częściowym aktywatorem receptora hormonu tarczycy; aktywacja tego receptora przez Rezdiffrę w wątrobie zmniejsza gromadzenie się tłuszczu w wątrobie.
Bezpieczeństwo i skuteczność leku Rezdiffra
Bezpieczeństwo i skuteczność preparatu Rezdiffra oceniano na podstawie analizy zastępczego punktu końcowego w 12. miesiącu w 54-miesięcznym, randomizowanym badaniu kontrolowanym placebo z podwójnie ślepą próbą. Zastępczy punkt końcowy mierzył zakres wątroba zapalenie i blizny. Sponsor jest zobowiązany do przeprowadzenia badania po zatwierdzeniu leku w celu sprawdzenia i opisania korzyści klinicznych ze stosowania leku Rezdiffra, co zostanie osiągnięte poprzez ukończenie tego samego 54-miesięcznego badania, które nadal jest w toku. Aby wziąć udział w badaniu, pacjenci musieli posiadać wątroba biopsja wykazująca stan zapalny wywołany NASH o stopniu umiarkowanym lub zaawansowanym wątroba blizny. W badaniu 888 pacjentów przydzielono losowo do grupy otrzymującej jeden z następujących leków: placebo (294 pacjentów); 80 miligramów leku Rezdiffra (298 pacjentów); lub 100 miligramów leku Rezdiffra (296 pacjentów); raz dziennie, jako uzupełnienie standardowej opieki w przypadku NASH, która obejmuje poradnictwo w zakresie zdrowej diety i ćwiczeń fizycznych.
Po 12 miesiącach biopsje wątroby wykazały, że większy odsetek pacjentów leczonych lekiem Rezdiffra osiągnął ustąpienie NASH lub poprawę w zakresie bliznowacenia wątroby w porównaniu z pacjentami, którzy otrzymywali placebo. W sumie u 26% do 27% pacjentów, którzy otrzymali 80 miligramów leku Rezdiffra i od 24% do 36% pacjentów, którzy otrzymali 100 miligramów leku Rezdiffra, doświadczyło ustąpienia NASH i braku pogorszenia bliznowacenia wątroby w porównaniu z 9% do 13% osób, które otrzymały otrzymało placebo oraz poradę dotyczącą diety i ćwiczeń fizycznych. Zakres odpowiedzi odzwierciedla różne odczyty patologów. Ponadto łącznie u 23% pacjentów, którzy otrzymali 80 miligramów leku Rezdiffra i od 24% do 28% pacjentów, którzy otrzymali 100 miligramów leku Rezdiffra, doświadczyło poprawy w zakresie wątroba blizny i brak pogorszenia NASH w porównaniu z 13% do 15% osób, które otrzymały placebo, w zależności od odczytów każdego patologa. Wykazanie tych zmian u odsetka pacjentów już po roku leczenia jest godne uwagi, ponieważ choroba zazwyczaj postępuje powoli, a u większości pacjentów potrzeba lat, a nawet dziesięcioleci, aby wykazać postęp.
Skutki uboczne Rezdiffry
Najczęstsze działania niepożądane leku Rezdiffra obejmowały biegunkę i nudności. Lek Rezdiffra zawiera pewne ostrzeżenia i środki ostrożności, takie jak polekowe toksyczne działanie na wątrobę i działania niepożądane związane z pęcherzykiem żółciowym.
Należy unikać stosowania leku Rezdiffra u pacjentów z niewyrównaną marskością wątroby. Pacjenci powinni przerwać stosowanie leku Rezdiffra, jeśli wystąpią u nich oznaki lub objawy pogorszenia wątroba funkcjonować podczas leczenia lekiem Rezdiffra.
Interakcje leków Rezdiffra
Stosowanie leku Rezdiffra jednocześnie z niektórymi innymi lekami, w szczególności statynami obniżającymi poziom cholesterolu, może powodować potencjalnie znaczące interakcje lekowe. Pracownicy służby zdrowia powinni zapoznać się z pełnymi informacjami dotyczącymi przepisywania leku, aby uzyskać dodatkowe informacje na temat potencjalnie znaczących interakcji leków z lekiem Rezdiffra, zalecanych dawkowań i modyfikacji sposobu podawania.
Połączenia FDA zatwierdziła lek Rezdiffra w ramach ścieżki przyspieszonej rejestracji, która umożliwia wcześniejsze zatwierdzenie leków stosowanych w leczeniu poważnych schorzeń i zaspokajających niezaspokojone potrzeby medyczne w oparciu o zastępczy lub pośredni kliniczny punkt końcowy, w przypadku którego istnieje uzasadnione prawdopodobieństwo przewidzenia korzyści klinicznej. Wymagane, wspomniane 54-miesięczne badanie, które jest w toku, oceni korzyść kliniczną po 54 miesiącach leczenia lekiem Rezdiffra.
Rezdiffra otrzymała w tym wskazaniu oznaczenia w ramach terapii przełomowej, szybkiej ścieżki i przeglądu priorytetowego.
Połączenia FDA udzielił zgody Rezdiffra spółce Madrigal Pharmaceuticals.
***
Źródło:
FDA 2024. Komunikat prasowy – FDA zatwierdza pierwsze leczenie pacjentów z bliznami wątrobowymi spowodowanymi stłuszczeniem wątroby. Opublikowano 14 marca 2024 r. Dostępne pod adresem https://www.fda.gov/news-events/press-announcements/fda-approves-first-treatment-patients-liver-scarring-due-fatty-liver-disease
***